Inleiding
De “92 stabiele elementen” verwijst naar de 92 natuurlijk voorkomende elementen in het periodiek systeem, beginnend bij waterstof (1) en eindigend bij uranium (92). Hoewel de term “stabiel” hier vaak wordt gebruikt, is het wetenschappelijk gezien nauwkeuriger om te spreken van de 92 (of soms 90-94) in de natuur voorkomende elementen, aangezien niet alle isotopen van deze elementen stabiel zijn (sommige, zoals uranium, zijn radioactief).
Hier zijn de belangrijkste feiten over deze groep elementen:
Definitie: Het gaat om de elementen met atoomnummer 1 (Waterstof) tot en met 92 (Uranium).
Natuurlijk vs. Stabiel: Van de eerste 92 elementen zijn de meeste stabiel, maar er zijn uitzonderingen. Technetium (43) en Promethium (61) komen bijvoorbeeld niet of nauwelijks stabiel in de natuur voor.
Primordiale elementen: Van deze 92 elementen zijn er 83 stabiel en hebben ze overleefd sinds de vorming van de aarde.
Radioactieve uitzonderingen: Uranium (92), Thorium (90) en Protactinium (91) zijn radioactief, maar hebben een zo lange halfwaardetijd dat ze nog steeds in de natuur voorkomen.
De grens: Uranium (92) werd lang beschouwd als het laatste en zwaarste natuurlijke element voordat de mensheid transuraan-elementen (elementen zwaarder dan 92, zoals Neptunium en Plutonium) begon te synthetiseren.
Structurele stabiliteit: IJzer (Fe, atoomnummer 26) wordt beschouwd als het meest stabiele element in termen van nucleaire bindingsenergie.
Hoewel er in de natuur sporen van zwaardere elementen (zoals plutonium-244) zijn gevonden, vormen de eerste 92 elementen de klassieke set van “natuurlijke” bouwstenen.
Radioactieve isotopen
Een isotoop van een element bestaat uit een zelfde aantal protonen, maar een verschillend aantal neutronen.
De zwakke kernkracht hoort net als de sterke kernkracht thuis in het rijtje van de fundamentele natuurkrachten: de sterke kernkracht, de elektromagnetische kracht, de zwakke kernkracht en de zwaartekracht. De relatieve grootte van de zwakke kernkracht zie je in figuur 1.
| Relatieve grootte | Omschrijving | Deeltjes die kracht overbrengen | |
| Sterke kernkracht | 1040 | Houdt protonen en neutronen in de kern bij elkaar | Gluonen |
| Elektromagnetische kracht | 1038 | Krachten tussen geladen deeltjes | Fotonen |
| Zwakke kernkracht | 1015 | Speelt een rol in vervalprocessen | W- en Z-Bosonen |
| Zwaartekracht | 1 | Houdt materie op grote schaal bij elkaar | Gravitonen (hypothetisch) |
Figuur 1: Overzicht van de vier fundamentele natuurkrachten en hun eigenschappen.
Veranderen van ‘smaak’
De zwakke kernkracht speelt alleen binnen de atoomkern een rol, net als de sterke kernkracht. Maar de zwakke kernkracht kan iets wat de sterke kernkracht niet kan: deze kan quarks van ‘smaak’ laten veranderen. De zwakke kernkracht kan een down-quark veranderen in een up-quark of andersom.
Doordat de zwakke kernkracht een quark van ‘smaak’ kan veranderen, kan deze een neutron (udd) laten veranderen in een proton (uud). Het krachtdeeltje dat hierbij een rol speelt is het W–boson. Bij de verandering stoot de atoomkern een W–boson uit. Dit boson is niet stabiel en splitst zich vervolgens op in een elektron (e-) en een anti-elektronneutrino . De elektronen die hierbij vrijkomen noem je β–straling.
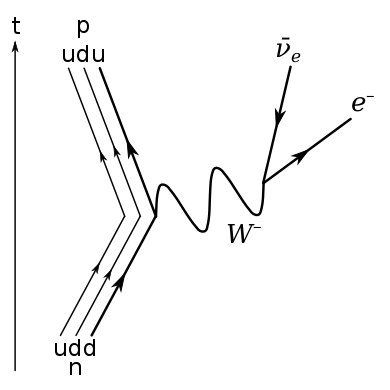
Figuur 2: Schematische voorstelling van het proces waarbij een neutron in de atoomkern verandert in een proton. Hierbij komt een W–boson vrij, dat opsplitst in een elektron (e-) en een anti-elektronneutrino. Dit proces noem je β–verval. Bron: Wikimedia.
Aangezien de massa van de kern van het atoom bij β–verval vrijwel gelijk blijft (aantal kerndeeltjes blijft gelijk en proton en neutron zijn ongeveer even zwaar), blijft het massagetal van het atoom in dat geval gelijk, maar neemt het atoomnummer wel met één toe (er zit nu één proton meer in de kern). Een voorbeeld hiervan is cesium (atoomnummer 55) dat wordt omgezet in barium (atoomnummer 56).
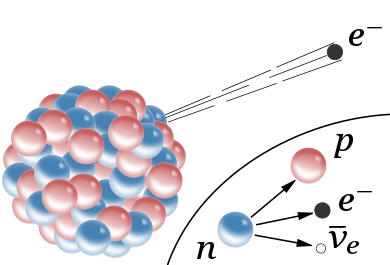
Figuur 3: Schematische weergave van β–verval. Bron: Wikimedia.
De zwakke kernkracht kan niet alleen een neutron in een proton laten veranderen. Deze kan ook een proton in een neutron laten overgaan door een up-quark te veranderen in een down-quark. Hierbij komt een W+-boson vrij en ontstaan een positron en een neutrino. Dit noem je β+-verval. Er is hiervoor wel voldoende energie nodig, omdat de massa van een neutron net iets groter is dan de massa van een proton. β+-verval kan daarom alleen spontaan optreden als de absolute waarde van de bindingsenergie van de oorspronkelijke atoomkern lager is dan die van de kern na verval. In dat geval bevindt de atoomkern zich na verval in een lagere energietoestand. De vrijgekomen energie is dan benut voor het bètaverval. Is dit niet het geval, dan zal er van buitenaf energie nodig zijn om dit proces in gang te zetten.
Aangezien de massa van de kern van het atoom bij β+-verval vrijwel gelijk blijft (aantal kerndeeltjes blijft gelijk en proton en neutron zijn ongeveer even zwaar), blijft het massagetal van het atoom in dat geval gelijk, maar neemt het atoomnummer wel met één af (er zit nu één proton minder in de kern). Een voorbeeld hiervan is natrium (Na, atoomnummer 11) dat wordt omgezet in neon (Ne, atoomnummer 10).
Hoewel de sterke en de zwakke kernkracht beide een rol spelen op atomaire schaal, is hun rol heel verschillend. De sterke kernkracht is heel krachtig en houdt alle deeltjes in de atoomkern mooi bij elkaar. De zwakke kernkracht is het zwakkere broertje dat in de atoomkern voor opschudding zorgt en radioactief verval veroorzaakt.
Met dank aan Auke-Pieter Colijn [1].
Gebruik in de ouderdomsmeting
Het gebruik van isotopen in ouderdomsmetingen, ook wel radiometrische datering genoemd, is een wetenschappelijke methode om de leeftijd van gesteenten, fossielen en archeologische vondsten te bepalen op basis van de constante snelheid van radioactief verval. Door de verhouding tussen de ‘moederisotoop’ (radioactief) en ‘dochterisotoop’ (stabiel vervalproduct) te meten, kan de tijd worden berekend die is verstreken sinds het materiaal is gevormd of het organisme is gestorven.
Hoe werkt radiometrische datering?
Radioactief verval: Onstabiele isotopen (radio-isotopen) vervallen met een constante, meetbare snelheid tot stabiele isotopen.
Halfwaardetijd: Dit is de tijd die nodig is voor de helft van de radioactieve atomen in een monster om te vervallen. Dit proces is onafhankelijk van uitwendige factoren.
Meten: Wetenschappers meten de verhouding tussen de resterende moederisotopen en de gevormde dochterisotopen met een massaspectrometer.
Belangrijke methoden en isotopen
Verschillende isotopen worden gebruikt, afhankelijk van de geschatte leeftijd van het materiaal:
Koolstof-14 (C) datering:
Toepassing: Geschikt voor organisch materiaal (hout, beenderen, textiel) tot ongeveer 50.000-60.000 jaar oud.
Principe: Zolang een organisme leeft, neemt het koolstof-14 op. Na de dood vervalt C tot stikstof-14 (N) met een halfwaardetijd van 5730 jaar.
Kalium-Argon (K-Ar) methode:
Toepassing: Gebruikt voor het dateren van zeer oude vulkanische gesteenten, vaak in combinatie met paleontologische vondsten.
Principe: Kalium-40 vervalt tot Argon-40 (halfwaardetijd van 1,25 miljard jaar).
Uranium-Lood (U-Pb) methode:
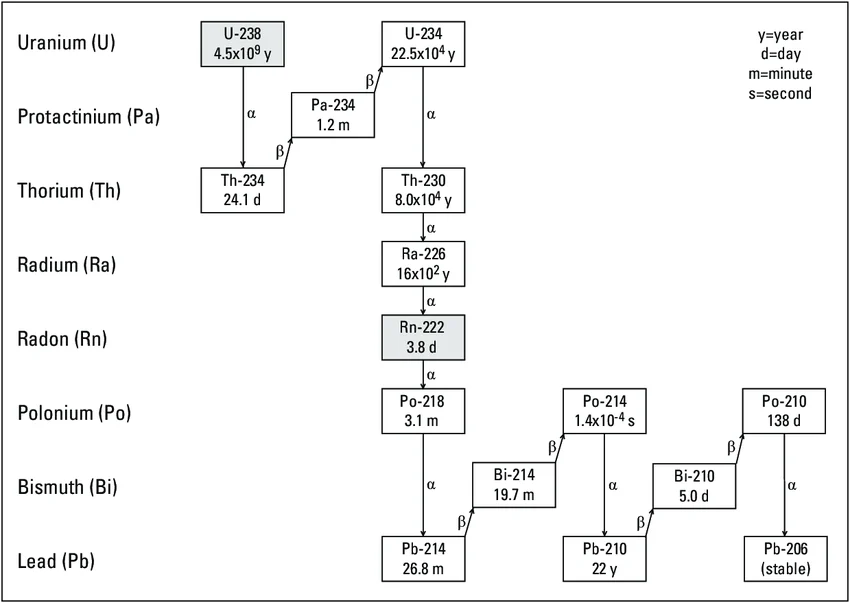
Toepassing: Zeer nauwkeurig voor het dateren van gesteenten die miljarden jaren oud zijn (bijv. de ouderdom van de aarde).
Toepassingen in de wetenschap
Geologie: Het bepalen van de ouderdom van aardlagen en de vorming van de aarde.
Archeologie: Het dateren van prehistorische artefacten en menselijke resten.
Paleontologie: Het vaststellen van de leeftijd van fossielen.
Radioactief verval onder extreme condities
Hier zit een interessante nuance in, want radioactief verval is een natuurkundig proces dat normaal gesproken volledig onafhankelijk is van externe omstandigheden. Maar er zijn een paar uitzonderingen — en die zijn fascinerend.
Laten we het helder en overzichtelijk maken.
Verandert radioactief verval onder extreme omstandigheden?
1. Alfa‑ en bètaverval: praktisch onveranderlijk
Voor de meeste isotopen (zoals uranium, kalium‑40, koolstof‑14):
Temperatuur → geen effect
Druk → geen effect
Chemische omgeving → vrijwel geen effect
Magnetische of elektrische velden → geen effect
Waarom?
Het verval wordt bepaald door krachten in de kern zelf. Externe omstandigheden beïnvloeden elektronen, maar niet de kern.
2. Uitzondering: elektronenvangst (electron capture)
Bij isotopen die vervallen door elektronenvangst kan de halfwaardetijd een klein beetje veranderen, omdat dit proces wél afhankelijk is van elektronen dicht bij de kern.
Voorbeelden:
Beryllium‑7
Ruthenium‑103
Tin‑121
Wat kan de halfwaardetijd beïnvloeden?
Zeer hoge druk (zoals in sterren of supernova’s)
Ionisatie (bijna alle elektronen verwijderen)
Extreem hoge temperaturen (plasma‑toestanden)
Maar zelfs dan gaat het meestal om veranderingen van enkele procenten, niet om ordes van grootte.
3. In sterren: extreme omstandigheden veranderen verval wél
In sterren en supernova’s gelden omstandigheden die op aarde onmogelijk zijn:
Temperaturen van miljoenen graden
Druk die miljarden keren hoger is dan op aarde
Volledig geïoniseerde atomen (geen elektronen meer)
Hierdoor kunnen:
Sommige isotopen sneller vervallen
Andere isotopen langzamer vervallen
Nieuwe vervalroutes ontstaan (bijv. protonvangst, neutronvangst)
Dit is belangrijk voor nucleosynthese — de vorming van elementen in sterren.
4. Voor ouderdomsbepaling op aarde: geen probleem
De isotopen die we gebruiken voor datering (C‑14, K‑Ar, U‑Pb, Rb‑Sr) zijn niet gevoelig voor normale aardse omstandigheden.
Daarom zijn radiometrische dateringen zo betrouwbaar.
Kort samengevat
Vervaltype Verandert onder extreme condities? Opmerkingen
Alfa‑verval Nee Kernprocessen, volledig stabiel
Bètaverval (β⁻) Nee Onafhankelijk van omgeving
Elektronenvangst Ja, een beetje Alleen bij extreme druk/ionisatie
Verval in sterren Ja, sterk Door plasma‑toestanden en hoge druk
Eindnoten
[1] https://www.natuurkunde.nl/artikelen/3694/zwakke-kernkracht-doet-wisseltruc

Geef een reactie